如何拓展新资源和独特资源来提高天然产物结构多样性、新颖性,以期发现更多创新药物新化学实体 (NCEs) 是当前天然药物化学工作者面临的一个关键问题。稀有濒危植物(Rare & Endangered Plants, REPs)是发现具有新颖结构和独特作用机制的创新药物的重要来源。
近期,胡金锋教授团队从我国特有的松科孑遗植物(渐危种)澜沧黄杉(Pseudotsuga forrestii Craib)枝叶中发现了2个具有新颖骨架结构的复杂九环五萜类化合物,分别命名为forrestiacids A (1)和B (2)。两者为立体化学异构体,系由一分子的重排螺环羊毛脂烷型三萜与一分子的松香烷二萜通过分子间Diels-Alder加成反应而形成的萜类杂二聚体(terpenoid hetero-dimers)。此类杂二聚体环系多、立体化学复杂,其结构(特别是绝对构型)是通过多种光谱/波谱技术、圆二色谱计算、单晶衍射和GIAO NMR化学位移计算辅以DP4+分析来得以确定。该类化合物是迄今为止NMR计算技术成功得以运用的研究对象中,分子量最大、结构最复杂的植物来源天然产物。
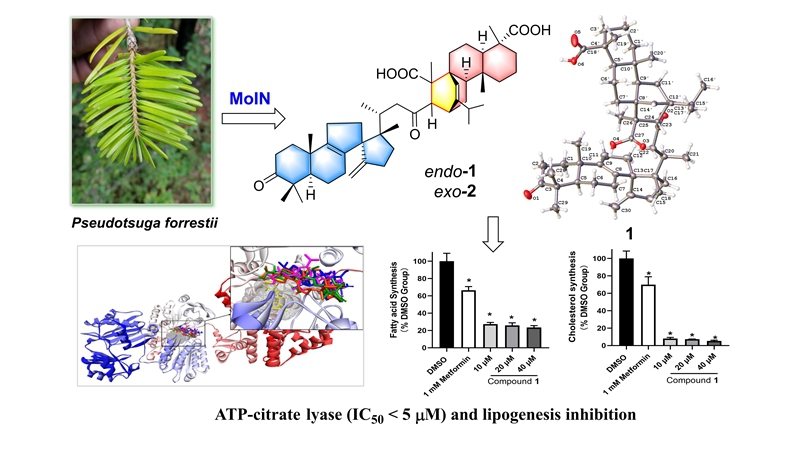
此类结构独特的九环五萜二酸类[4+2]-加合物是通过基于分子网络技术(Molecular Ion Networking, MoIN)的化学成分定向挖掘而获得的。近年,基于LC-MS发展起来的MoIN技术能极大地提高天然产物的分离效率和分离成本,避免了传统分离方法的盲目性和重复性。借助MoIN技术,可以在分离前期快速找到目标化合物所在部位,锁定结构新颖的目标成分,实现高效导向分离。
高脂血症(hyperlipidemia)是引发心血管疾病的重要因素。ATP-柠檬酸裂解酶(ACL)是近年备受关注的高脂血症新靶标,目前已有一个合成小分子(二羧酸类)药物(bempedoic acid)于2020年批准上市。本研究中,对forrestiacids A 和B 针对糖脂代谢疾病相关多个靶点开展了活性筛选,发现对ACL具有较强的抑制活性,两者IC50值分别为4.12和3.57 μM。进一步研究发现forrestiacid A可显著抑制HepG2细胞中脂质(脂肪酸和胆固醇,10 μM时抑制率分别为72.7%和92.0%)的从头合成,提示在降血脂药物研发方面具有重大开发潜能。
Forrestiacids可显著抑制脂质合成,但ACL抑制活性似乎并不是特别强(< 5 μM)。继而对forrestiacids与ACL及其他脂质合成密切相关靶蛋白进行了分子对接研究,发现它们与ACL, ACC, FAS 和 SCD1的配体结合域均表现出较好的结合亲和力,提示其表现出的脂质合成强抑制活性可能与调控了ACL、ACC等多个靶蛋白有关。此外,与ACL的对接结果表明,其结合位点位于柠檬酸结合位点的外侧口袋,提示ACL中可能存在变构位点。值得一提的是,forrestiacid A的分离量达到克级以上,可为后续体内外活性及构效关系研究提供足量的样品。
本工作独辟蹊径地利用我国特有稀有濒危植物资源,及时确认它们潜在的重大药学价值,以期使那些珍贵物种受到重视和科学保护以利其持续为人类利用,具有重大研究价值与应用前景。相关成果近日发表于化学领域顶尖期刊Angewandte Chemie International Edition。
我院天然药物学系熊娟副教授为该论文第一作者,胡金锋教授和中科院上海药物研究所李佳研究员为本论文共同通讯作者,台州学院珍稀濒危植物园协助提供植物样品,美国南卡罗来纳医科大学Hamann教授协助使用超级计算机开展化学位移计算。本研究获NSFC重点项目和面上项目的资助。
原文链接:https:doi.org/10.1002/anie.202109082


