我院药物化学系王任小研究员与李嫣副研究员多年来选择难度较大的蛋白-蛋白相互作用体系(protein-protein interactions, PPI)作为药物靶标开展科研攻关。近日,该团队在新型BAX蛋白激动剂研发领域取得进展,相关成果分别发表于药物化学权威期刊Journal of Medicinal Chemistry和综合性权威期刊Journal of American Chemical Society Au。
BAX蛋白是细胞凋亡通路的关键执行者,直接激活BAX可绕过肿瘤细胞对传统BCL-2抑制剂的耐药机制,因而成为抗癌药物研发的前沿方向。然而,迄今报道的BAX小分子激活剂结构类型极为有限,成药性不佳,其激活机制也尚不明确,制约了相关药物的研发。
为了获得新结构类型的BAX蛋白激活剂,该团队首先针对BAX蛋白Trigger位点开展虚拟筛选,从160万化合物库中成功获得活性苗头分子。通过对原始复杂骨架进行“骨架跃迁”与多轮结构优化,最终获得了一类具有苯基吡咯骨架的化合物。经过系统性的生物学评价,该系列中编号27c的化合物表现尤为突出:它能以亚微摩尔级亲合力(IC50 = 300 nM)结合BAX蛋白,而对BCL-2、BCL-XL、MCL-1等其他抗凋亡蛋白的亲合力较弱,显示出良好的靶向选择性。在细胞层面,27c有效诱导BAX发生激活所需的构象变化,促使其从细胞质转位至线粒体,进而引发线粒体膜电位丧失、细胞色素c释放,并最终激活Caspase凋亡通路级联反应,在多种急性髓系白血病细胞中展现了显著的增殖抑制活性。整体而言,该化合物的生物活性略优于已知的最佳BAX激活剂。值得一提的是,对于因BCL-XL等高表达而产生耐药性的实体瘤细胞,27c与BCL-XL抑制剂(如Navitoclax)联用可产生协同增效,显著增强杀伤效果,为未来联合治疗策略提供了有力支持。
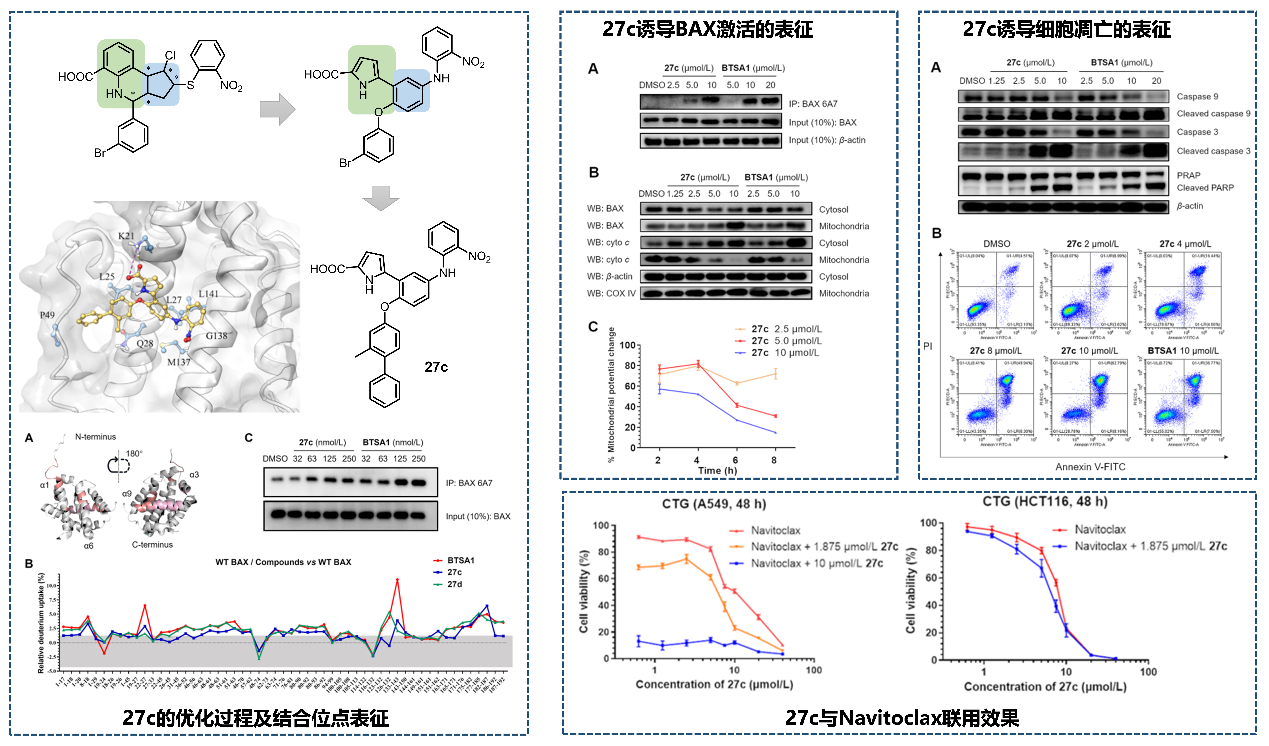
图-1:苯基吡咯类BAX蛋白激活剂的优化设计与生物活性研究
为了在微观层面诠释化合物27c激活BAX蛋白的作用机制,该团队创新性地将微扰弹性带(NEB)方法与马尔可夫状态模型(MSM)相结合,从动力学与热力学双重视角完整重构了BAX蛋白激活的全景动态过程,并系统比较了化合物27c与天然激活肽Bim在诱导BAX活化过程中的异同。模拟结果表明:两者虽均结合于BAX的trigger位点并启动激活,但其驱动的后续构象变化路径和效率存在根本差异:Bim通过跨越较高能垒实现不可逆的α9螺旋释放,建立起高度协同的全局变构网络;而27c虽能快速引发初期构象变化,却无法维持α9螺旋的解离状态,仅产生局部、低协同性的可逆波动,因而难以有效启动下游寡聚化。该机制研究不仅从理论层面解释了BAX小分子激活剂的活性特点,也为未来设计能更有效模拟天然肽、实现完全激活的下一代BAX激动剂提供了关键的理论指导。
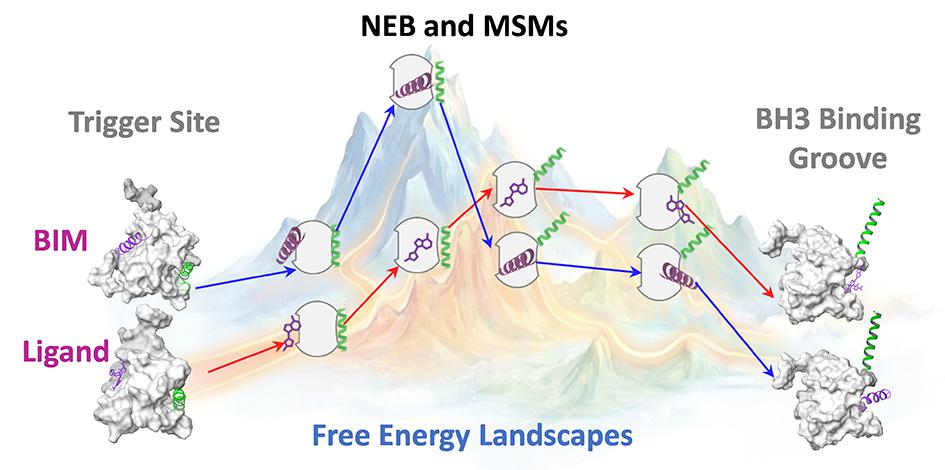
图-2:Bim多肽和化合物27c诱导BAX蛋白激活的最小自由能路径展示
上述两项研究由王任小研究员、李嫣副研究员、周璐教授共同指导,博士生蔡卫、硕士生赵美玲等团队成员分别完成核心实验与计算模拟等工作。该项研究得到国家自然科学基金、科技部国家重点研发计划、上海市科委等项目的资助。
原文链接:
(1)Cai W et al. Design, Synthesis, and Evaluation of Phenylpyrrole Derivatives as Small-Molecule Activators of BAX, J. Med. Chem., 2026, ASAP. https://pubs.acs.org/doi/10.1021/acs.jmedchem.5c02670
(2)Zhao, M. L. et al. Combined Nudged Elastic Band and Markov State Models Uncover Distinct BAX Activation Pathways by Bim Peptide and a Small Molecule”, J. Am. Chem. Soc. Au., 2026, 6, 1228−1237. https://pubs.acs.org/doi/10.1021/jacsau.5c01620.


