在冷肿瘤的免疫微环境特征背景下,PROTACs展现出独特的优势,包括解决耐药问题和不可成药靶点等。而针对免疫抑制微环境的独特性和复杂性的靶向PROTAC给药系统仍缺乏完备的指导性综述。因此,针对“冷肿瘤”的免疫治疗现状及基于PROTAC递药系统设计的最新进展,本文期望可以提供一种新的冷肿瘤治疗范式。相关成果以PROTAC Delivery in Tumor Immunotherapy : Where Are We and Where Are Going?为题,在线发表于国际知名期刊 Journal of Controlled Release。
近年来,随着“冷肿瘤”概念的提出,人们逐渐清楚地认识到传统的小分子药物在实现对这些肿瘤的选择性靶向方面存在困难。它们大多以“占据驱动”为作用机制,治疗过程中常存在效率低下、脱靶毒性等问题。而PROTAC的出现,为人们提供了冷肿瘤免疫治疗的新思路。
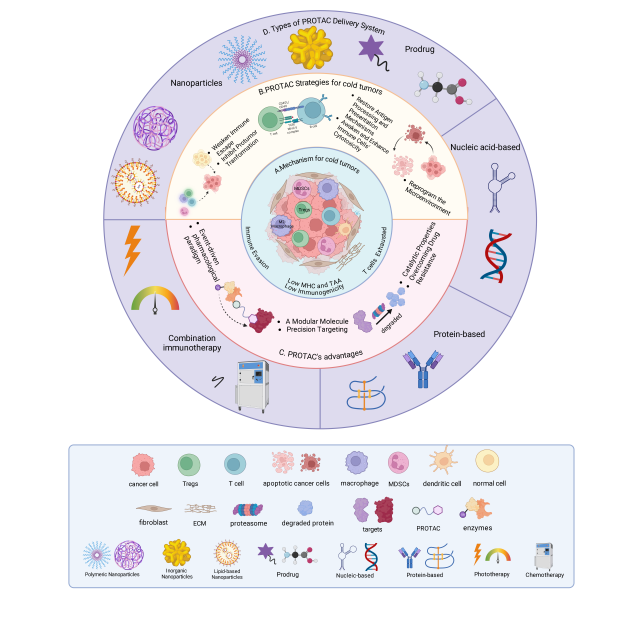
冷肿瘤免疫治疗策略示意图,概述了冷肿瘤免疫抑制微环境的特点、PROTAC疗法的潜在应用、PROTAC疗法的优势、PROTAC的不同递送系统以及设计这些递送系统的原则
本文首先对冷肿瘤免疫治疗进行了详尽的叙述,总结了冷肿瘤形成的原因,强调了使用免疫疗法治疗冷肿瘤的挑战和迫切需要开拓创新的治疗策略来对抗免疫逃避。随后,课题组转向PROTACs(蛋白降解靶向嵌合体),阐明该类分子具有的“事件驱动”机制,以及其降解“不可成药靶点”的潜力,揭示了PROTAC在冷肿瘤治疗策略开发中的应用前景。
然而,由于溶解性差、渗透性低、系统生物利用度低、生物分布非特异性以及Hook效应等问题,大多数PROTAC分子难以进入人体临床试验。而药物递送系统能够有效改善PROTAC分子的一些局限性,主要包括提高其物理化学性质,以及作为运输载体增加组织特异性。
因此在最后,本文重点介绍了多种PROTAC递送系统,包括纳米颗粒、前药策略、基于蛋白质和核酸的递送系统,以及这些PROTAC递送系统在新药研究开发中的具体应用。这些药物递送系统能够装载PROTAC分子,增加其在体内的有效浓度,并延长其循环时间,提高稳定性和持久性,使得PROTAC能够针对性地作用于特定的病变部位,增强治疗的针对性。同时本文还讨论了设计这些递送系统时需考虑的原则,以及如何通过这些系统实现PROTAC技术从实验室到临床应用的转化。本篇综述引用近150高水平文献,对此领域近十年的研究进展进行了详尽综述,对本领域的研究具有实际的参考价值。
复旦大学药学院22级本科生李依阳、吴亦可、高斯涵为本文的共同第一作者,孙涛副教授、蒋晨教授为论文的通讯作者。该研究工作获得国家重点研发计划、国家自然科学基金等项目支持。这是学院继2023年21级本科生一作发表Acta Pharm Sin B(第一作者:瞿炀芪、张桐、许兢菁,通讯作者孙涛、蒋晨)论文后另一标志性事件。
原文链接:https://www.sciencedirect.com/science/article/pii/S0168365924008356?via%3Dihub


