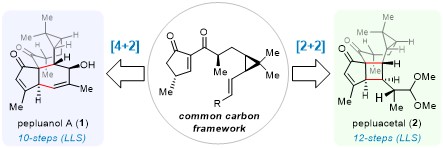
复旦大学药学院孙域课题组近期完成了大戟二萜pepluanol A及pepluacetal的发散性全合成,相关成果以Divergent Syntheses of the Euphorbia Diterpenoids Pepluanol A and Pepluacetal为题,在线发表于权威期刊Journal of the American Chemical Society。

大戟二萜(Euphorbia diterpenoids)是从中国传统药用植物大戟属(Euphorbia genus)中分离的一类天然产物,具有复杂碳骨架、密集立体中心和广泛生物活性,是全合成的热点目标。2016年,邱明华团队从传统草药斑地锦(E. peplus)中分离出Pepluanol A、B及Pepluacetal,并于2018年进一步发现Pepluanol C、D(图1)。这些化合物结构独特,并可通过靶向Kv1.3通道展现免疫抑制活性,对自身免疫疾病有潜在治疗价值。由于该类天然产物复杂而独特的结构及良好的应用前景,Pepluanol二萜成为全合成的热点。
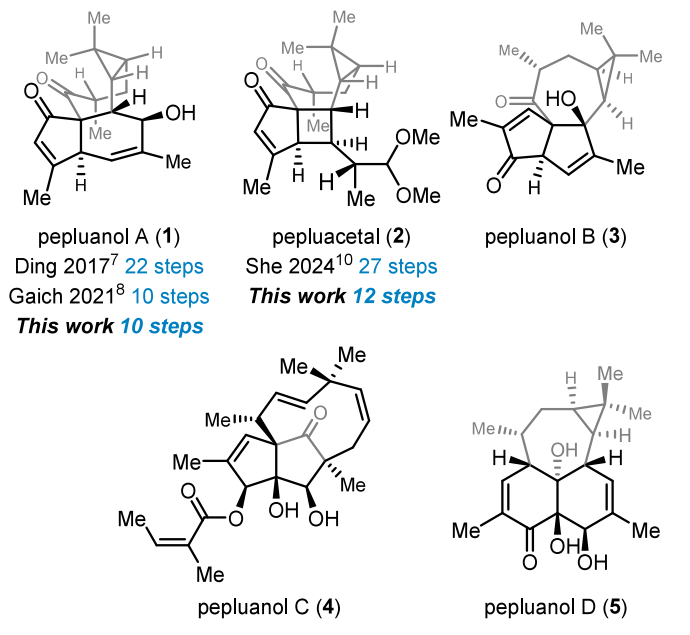
图1:Pepluanol家族天然产物
复旦大学孙域团队通过采用发散性合成策略,利用多种光化学反应,成功实现了天然产物Pepluanol A及 Pepluacetal的高效合成(图2)。其中,Pepluanol A的合成采用[4+2]Diels-Alder反应作为骨架合成的关键策略,而Pepluacetal采用光促进的[2+2]环加成反应构筑天然产物的核心骨架。两条合成路线均采用Mortita-Baylis-Hillman反应实现前体的构筑,并分别通过HWE烯化反应或Julia-Kocienski烯化反应实现片段链接,进而追溯到共同中间体醛14。14可通过臭氧化反应切断烯醇甲醚15,由Baran课题组合成的中间体16制备。值得一提的是,本工作与2021年Gaich团队Pepluanol A的合成采用了相同的起始原料,但其Diels-Alder策略采用了完全不同的切断方式。
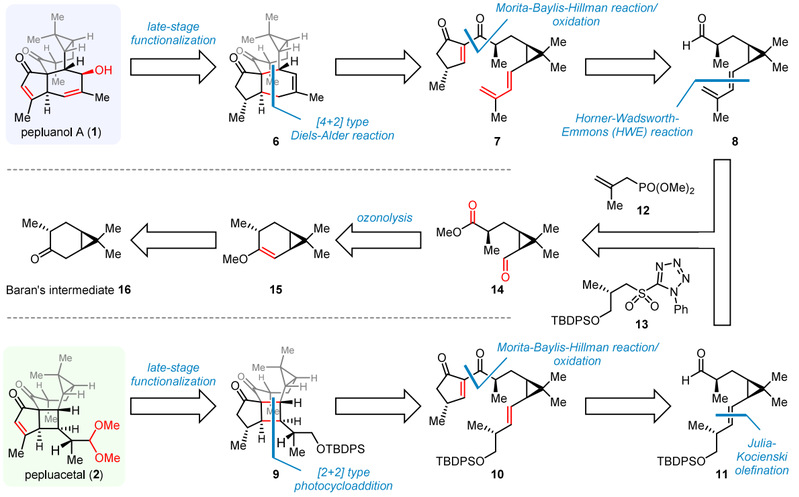
图2:Pepluanol A及Pepluacetal的逆合成分析
根据逆合成方案,孙域团队开展了Pepluanol A的全合成(图3)。从商品化的(+)-3-蒈烯出发,经三步反应可制得Baran中间体16。将16经KHMDS/MeOTf处理制得烯醇甲醚15后,直接进行臭氧解反应,以54%两步收率得到关键醛中间体14。随后通过HWE反应将14与磷酸酯17连接,以89%收率和>98:2的E/Z选择性构建二烯化合物17。经DIBAL-H还原得到醛8,后者与烯酮18经Morita-Baylis-Hillman反应连接,再经Dess-Martin氧化原位生成[4+2]前体7。该产物可自发进行分子内Diels-Alder反应,以63%收率和>98%非对映选择性得到目标产物6。推测C16位的甲基的位阻取代对[4+2]转化的面选择性起到了关键作用。值得一提的是该反应需在低浓度(0.005 M)下进行以抑制分子间DA等副反应。
通过一锅法Saegusa-Ito氧化条件可顺利实现A环烯酮的构建,以81%收率得到19。但后续的光诱导烯反应遇到显著挑战:常规光催化剂(如TPP、Rose Bengal)均不能使19转化;亚甲基蓝仅导致微量烯烃异构体20生成(约10%)并伴随严重分解。采用光氧化还原催化剂Ir(dtbbpy)(ppy)2PF6时,在乙腈中反应转化率仅30%。受罗佗平课题组在vinigrol全合成中氘代溶剂效应的启发,研究团队将溶剂更换为氘代乙腈后,烯反应转化率提升至>98%,分别以24%和65%的收率获得目标产物Pepluanol A(1)及其异构体20。最后通过Shenvi团队的HAT异构化方法,可将20以84%收率转化为1。
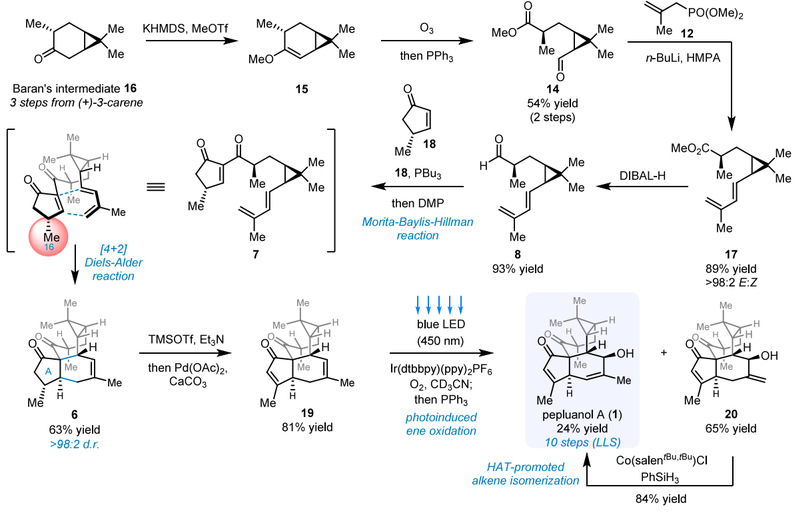
图3:Pepluanol A的10步全合成
在完成对pepluanol A(1)的全合成后,研究团队进一步开展了pepluacetal(2)的合成研究(图4)。基于发散性设计,以共同中间体14为起点,经两步Julia−Kocienski烯基化/还原可得到醛11,总收率82%,E:Z选择性8:1。参照化合物1的合成路线,11与烯酮18经Morita−Baylis−Hillman反应后,用PDC原位氧化得到烯二酮10。该化合物室温易分解,需立即使用。在[2+2]光环加成中,254、365、390或450 nm照射均未得到目标产物,而310 nm照射可高效转化为单一非对映异构体9(两步收率47%)。该反应与合成1中的[4+2]环加成类似,具有立体专一性,。值得一提的是,该反应未观察到竞争性的[5+2]型环加成产物。
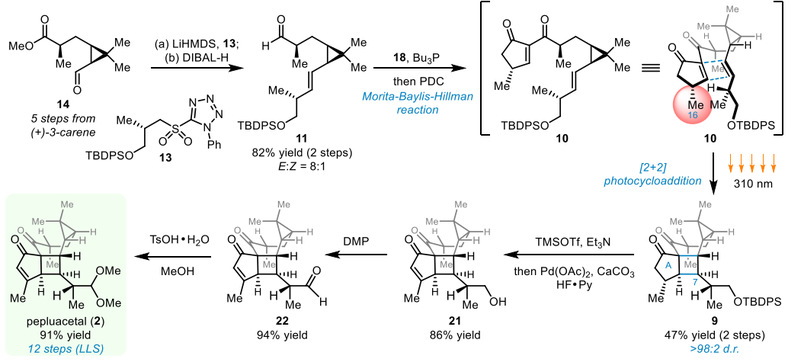
图4:Pepluacetal的12步全合成
全合成研究的开展为后续的活性研究奠定了基础。项目团队获得了一系列具有复杂结构与潜在生物活性的天然产物及其类似物。通过与交通大学仁济医院杨帆课题组合作,项目团队证实了该类化合物具有抗肺纤维化活性(图5)。小鼠原代肺成纤维细胞中的抗纤维化活性测试表明:化合物20、9和21对纤连蛋白表达表现出强抑制活性(IC50分别为7.04 μM、6.53 μM和3.60 μM);化合物2和19亦具显著效果(IC50为11.78 μM和14.66 μM);其余化合物无明显活性(IC50 > 20 μM)。值得注意的是,天然产物1和2的活性弱于其合成衍生物20和21,这为该类化合物的结构优化与活性研究提供了重要依据。
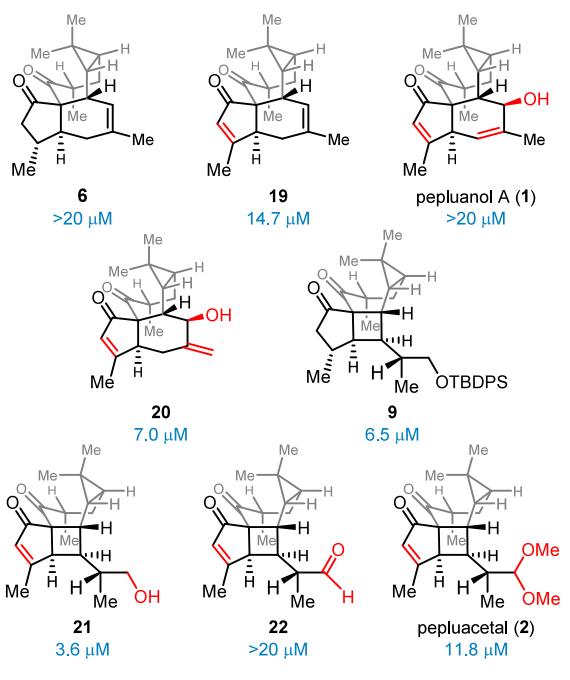
图5:构效关系与活性研究
总结
本工作从共同中间体出发,完成了结构复杂的大戟烷型二萜pepluanol A(1)和pepluacetal(2)的发散性全合成。路线分别以10步通过分子内Diels−Alder [4+2]环加成策略合成1(已报道合成路线10-22步),以12步通过立体选择性光促进的[2+2]环加成制备2(已报道合成路线27步)。两部分合成工作均体现了良好的路线简洁性与精准的立体化学控制。后续合作开展的活性研究首次揭示了该类化合物具有抗肺纤维化活性,这为该类中药提取物的活性成分研究及其药用价值的深入挖掘创造了有利条件。
这一成果近期发表在Journal of the American Chemical Society期刊上,复旦大学孙域青年研究员为论文的最后通讯作者。项目共同通讯作者为上海交通大学仁济医院杨帆教授。复旦大学药学院硕士生邱东垣、赵梓晗为该论文的共同第一作者。该工作获得国家自然科学基金面上项目等资助。
原文链接:https://pubs.acs.org/doi/10.1021/jacs.6c01271
TOC