2022年4月12日,国际顶级肿瘤学期刊《Cancer Discovery》(IF 39.4)在线发表复旦大学附属中山医院樊嘉院士团队与复旦大学药学院朱棣课题组合作的最新药理学研究成果“干扰素α改善糖代谢和免疫微环境”,该研究开展了干扰素α和PD-1抗体联用的药理学机制研究,为肝细胞癌(HCC)的治疗提出了一种提高抗PD-1抗体疗效的联合治疗新策略。

干扰素α在临床已有数十年的使用历史,在病毒防治、免疫调节等领域其应用价值已得到充分肯定,使得大量患者获益。但因其作用广泛、模式多样,单药抗肿瘤疗效欠佳,如何在特定肿瘤免疫治疗中合理使用干扰素α成为极具临床研究价值的重大科学问题。
在这项最新肿瘤药理学研究中,团队构建了小鼠自发性肝癌模型与原位移植瘤模型,均显示联合治疗组小鼠肿瘤明显缩小、肺转移减少、生存期显著延长。研究团队又进一步运用流式质谱技术(CyTOF)详细地剖析了不同治疗组肿瘤微环境中浸润的各亚群淋巴细胞,发现CD27+CD8+T细胞这一具有强大免疫杀伤功能的亚群在联合治疗后的肝癌组织中浸润明显增加,是响应联合治疗从而产生抗肿瘤效应的关键亚群。此外,基于公共单细胞数据集的分析证据亦支持这一发现:在多种实体肿瘤中,免疫治疗响应的患者中CD27+CD8+T细胞比例显著升高。
干扰素α正是通过作用于肿瘤细胞一侧,激活胞内IRF1并诱导其入核阻遏FosB基因转录;在FosB表达缺失状态下,糖酵解关键因子HIF1α的转录活性明显下降,导致肝癌细胞对微环境中葡萄糖的摄取与利用能力显著受限,从而有效改善微环境糖代谢失衡状态。由此产生的富葡萄糖微环境可激活CD8+T细胞中mTOR信号并形成mTOR-FOXM1调控轴,诱导CD27基因表达,从而增强浸润CD27+CD8+T细胞的比例。
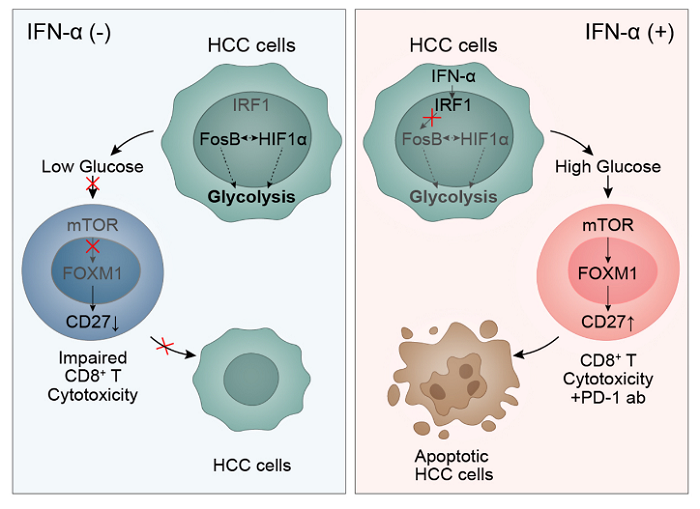
理作用机制图:IFN-α抑制HCC肿瘤细胞的葡萄糖代谢,同时增加T细胞的糖酵解,从而通过促进PD-1阻断诱导的免疫反应来提高T细胞的细胞毒能力。
药学院药理系2020级博士生刘成龙为该论文共同第一作者,他依托药学院所在课题组的肿瘤免疫药物发现平台,揭示了肿瘤免疫药理学机制,发现CD27+CD8+ T细胞在本身具有出众杀伤与增殖潜能的同时,也高表达PD-1这一经典“刹车分子”,使得其在干扰素单药使用时并不能获得充分扩增,限制了干扰素α单药的作用。而PD-1抗体则可有效解决这一问题,这也解释了为什么干扰素与免疫检查点抑制剂可以形成完美联动,在动物模型与临床患者中均展现出优异的组合疗效。
复旦大学附属中山医院樊嘉院士、复旦大学朱棣(近期已调动至基础医学院)、附属中山医院徐泱为该文共同通讯作者。该工作获得了国家自然科学基金委,上海市科委自然科学基金等支持。


