近期,复旦大学药学院陆伟课题组设计了一种细菌仿生癌症疫苗佐剂,相关成果以《Bacterium-Mimicking Vector with Enhanced Adjuvanticity for Cancer Immunotherapy and Minimized Toxicity》为题,在线发表于国际知名期刊《Advanced Functional Materials》(IF 15.621)。
癌症的免疫治疗是继手术、放疗、化疗后的新兴疗法,近年来取得了显著的临床治疗效果,为癌症的治愈带来新希望。它可通过局部注射癌症疫苗激活患者的免疫系统,特异性地杀伤肿瘤细胞。癌症疫苗由肿瘤特异性抗原和免疫佐剂组成。其中,研发能够产生高效、持久抗肿瘤免疫效力的免疫佐剂是癌症疫苗成功的关键。但是,增加佐剂效力通常伴随着毒性的增强。例如完全弗氏佐剂,它的主要成分为热灭活的分枝杆菌(如卡介苗菌),尽管它在佐剂效力方面被认为是金标准,但其严重的反应原性和毒性使其仅被应用于兽用疫苗,而不能在人体中使用。一些临床试验或使用的佐剂虽然安全,但其效力又显著不如弗氏佐剂。因此,研发高效低毒的免疫佐剂一直以来是疫苗研究领域的难点,同时也具有重要的临床意义。
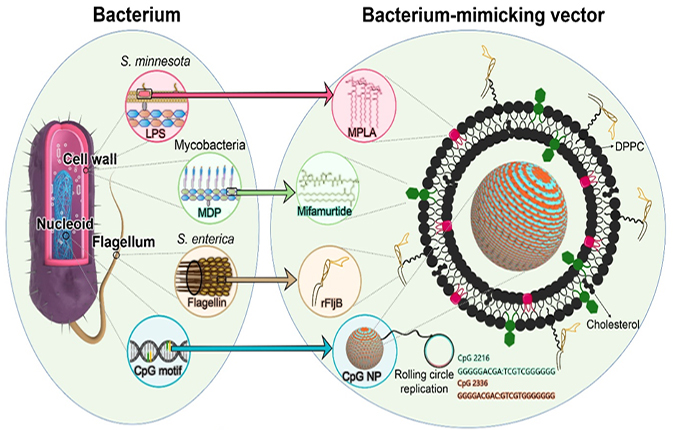
团队研究人员根据细菌的构造,采用仿生策略将来自于多种细菌不同细胞结构的佐剂活性成分整合于一体,以发挥协同的免疫刺激作用。将沙门氏菌细菌脂多糖减毒成分单磷酰脂质A和分枝杆菌胞壁酰二肽的类似物米伐木肽嵌入脂质体磷脂双分子层中,模拟细菌细胞壁;脂质体表面连接重组表达的沙门氏菌鞭毛蛋白,模拟细菌鞭毛;脂质体包载含有非甲基化胞嘧啶鸟嘌呤二核苷酸序列的DNA纳米颗粒,模拟细菌拟核,制备得到细菌仿生癌症疫苗佐剂。它能够通过多条信号通路激活免疫系统,对小鼠黑色素瘤的治疗和预防效果显著优于弗氏佐剂。更重要的是,该免疫佐剂与光热治疗相结合可作为光热自体肿瘤疫苗,一方面通过光热物理治疗杀死患者肿瘤细胞;另一方面,利用被杀死的肿瘤细胞所释放的肿瘤特异性抗原,结合免疫佐剂激发机体的免疫反应,杀死残余肿瘤细胞,达到根治肿瘤和预防肿瘤复发的目的。该光热自体肿瘤疫苗可治愈50%的小鼠黑色素瘤且不再复发。
该细菌仿生脂质体在给药后仅产生轻微、短暂可逆的刺激性,注射部位的佐剂可完全被吸收。与之相比较,弗氏佐剂由于采用石蜡油作为剂型辅料,在注射部位的油滴不能被降解,引起肉芽肿等病变,产生长期的毒性。同时,弗氏佐剂采用的灭活细菌不可避免的产生强烈的局部刺激性,且佐剂成分来自细菌或其代谢物,组成不明确,制剂批次间的质量可控性较差,潜在的毒性风险难以控制。由于本研究设计的细菌仿生脂质体包载的四种佐剂成分均为人工合成,且分别在动物或临床试验中被证实为安全低毒,脂质体剂型亦为药用注射剂型,因此该细菌仿生免疫佐剂具有高效、可吸收、安全、成分可控的优点,具有潜在的临床转化价值。
复旦大学药学院郑彬彬为该论文的第一作者。复旦大学药学院陆伟教授和上海交通大学医学院肖泽宇教授为该论文的共同通讯作者。该研究获得国家自然科学基金项目和上海市优秀学术带头人计划资助。
全文链接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.201901437


