炎症性肠病(Inflammatory bowel disease, IBD)是一类发病率日益增长的全球性肠道炎性疾病,严重影响病人的生活质量。目前的治疗药物如5-氨基水杨酸(5-Aminosalicylic acid, 5-ASA)、皮质类固醇和抗肿瘤坏死因子-α单克隆抗体等,虽能缓解症状,但无法实现完全缓解且存在副作用。人类胃肠道栖息着数以万亿计的微生物,肠道微生物群在维持宿主稳态中起到至关重要的作用,其失调是IBD的关键标志。因此,调节肠道微生物群成为IBD治疗的新策略。
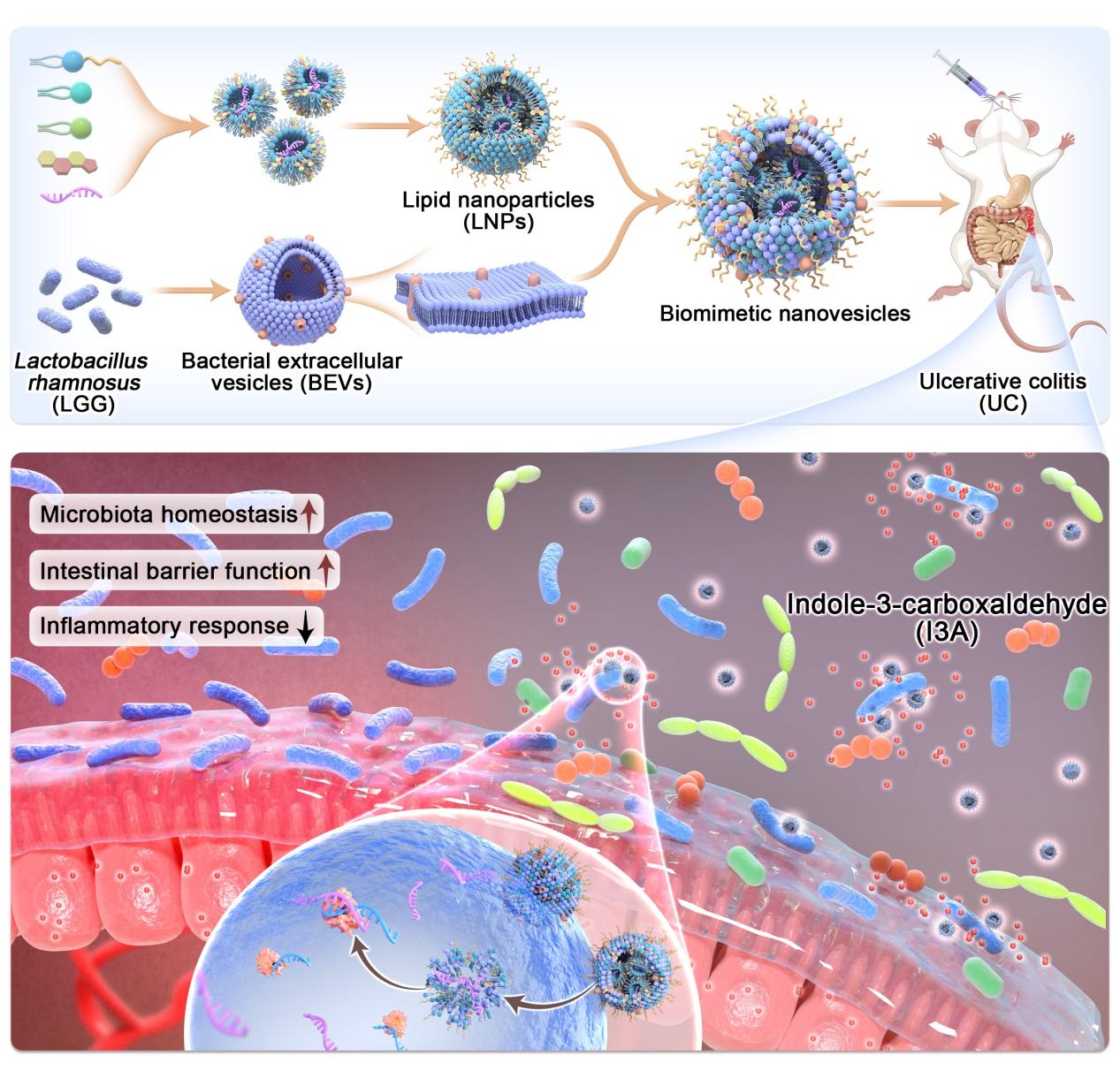
近日,复旦大学药学院戚建平课题组在Science Advances期刊发表最新研究成果“miRNA-loaded biomimetic nanoparticles orchestrate gut microbe to ameliorate inflammatory bowel disease”,报道了一种能够对共生菌鼠李糖乳杆菌进行改造的仿生纳米颗粒。通过将鼠李糖乳杆菌来源的细菌胞外囊泡(Bacterial extracellular vesicles, BEV)与脂质纳米粒(Lipid nanoparticles, LNP)进行功能化结合,制备了细菌胞外囊泡-脂质纳米粒(BEV-LNPs)。该纳米载体对鼠李糖乳杆菌的靶向效率显著高于大肠杆菌。体内外稳定性实验表明,相较于传统脂质纳米粒,BEV-LNPs在模拟生理介质及胃肠道环境中展现出更佳的稳定性。将该纳米载体与5-ASA联合使用时,促进了鼠李糖乳杆菌的增殖并增加了吲哚-3-甲醛的生成量,在急性和慢性结肠炎模型中均显著改善了治疗效果,有效减轻肠道炎症,修复受损肠道上皮屏障,并促进肠道菌群重新恢复平衡。
该课题基于IBD患者肠道菌群失调这一严重危害肠道健康的现象,创新性提出口服递送miRNA的方法,通过基因调控作用,逆转肠道菌群失衡,补充有益代谢物,恢复IBD患者的肠道屏障,改善结肠炎。该仿生载体能够克服传统化学药物治疗方法所带来的全身毒副作用和病灶部位蓄积量不足,疗效不够等问题,探究了肠道菌群的开发利用,为IBD治疗提供了一种安全有效的策略。
复旦大学药学院博士生刘文娟为本文的第一作者,复旦大学药学院教授戚建平为本文的通讯作者。该工作获得了国家自然科学基金和上海市科学技术委员会等基金项目的支持。
原文链接:https://www.science.org/doi/10.1126/sciadv.adw5984