线粒体作为细胞的“能量工厂”,在维持细胞能量稳态、氧化应激等方面发挥重要作用。由于大脑高能耗需求,神经元线粒体数量往往是外周体细胞的几十至数百倍。线粒体自噬是细胞选择性清除受损线粒体、维持线粒体群体健康和能量稳态的关键事件。线粒体自噬包括受损线粒体被自噬小体包裹并最终运送到溶酶体降解等步骤,通常涉及三种类型线粒体自噬中间体:线粒体、线粒体自噬体和线粒体溶酶体。线粒体自噬中间体数量比例变化和空间分布特征不仅与神经元能量稳态维持、氧化应激损伤保护密切相关,在神经退行性疾病进展过程中也发挥重要作用。
在阿尔茨海默症(AD)发展过程中,线粒体自噬水平降低不但与线粒体损伤、细胞能量供应短缺、毒蛋白沉积等事件密切相关,还往往早于认知障碍等典型症状出现。研究表明,线粒体自噬诱导药物能够降低AD淀粉样蛋白和Tau蛋白病理沉积,增强小胶质细胞吞噬功能,缓解AD相关认知障碍。因此,可视化活细胞内线粒体自噬水平及其关键中间体对于了解AD发病机制和药物筛选具有重要意义。首先,线粒体自噬功能障碍通常源于其关键过程受阻;其次,不同药物对线粒体自噬中间体的影响各不相同。因此,可视化胞内线粒体自噬中间体的数量比例和空间分布,有助于全面评估线粒体自噬进程,提高线粒体自噬诱导剂筛选效率。
目前,超分辨荧光显微镜成像技术虽能观测活细胞线粒体自噬水平,但仍存在多重荧光染色操作复杂、光谱重叠干扰信号解析,以及潜在细胞毒性等问题,导致难以同步、精准地识别关键自噬中间体,也无法定量研究自噬损伤的具体步骤。因此,实现活细胞线粒体自噬中间体的连续、同步、定量可视化是该领域亟待解决的问题。
近日,复旦大学药学院李聪教授、游艳青年研究员,复旦大学信息科学与工程学院余锦华教授,及云南大学药学院雷祖海教授联合研究团队在Nature Communications(自然-通讯)杂志发表了题为:“An AI-assisted fluorescence microscopic system for screening mitophagy inducers by simultaneous analysis of mitophagic intermediates”(人工智能驱动荧光显微成像系统可视化线粒体自噬中间体筛选线粒体自噬诱导剂)的研究论文。该工作开发了一种AI辅助荧光显微成像系统(AI-FM),用于活细胞线粒体自噬流的实时、动态、定量评估。AI-FM系统将具有线粒体靶向性的pH比率响应荧光探针Mcy3与深度学习模型有机结合,实现线粒体自噬中关键中间体的准确识别,并提供胞内各类中间体分布、密度、比例等定量信息,平均检测准确率高达86%。研究人员利用AI-FM系统筛选出一种新型线粒体自噬诱导剂Y040-7904。该化合物能够促进受损线粒体向自噬小体转运,并提高神经元线粒体自噬水平。在AD神经元细胞模型和AD线虫模型中,Y040-7904通过激活SIRT1/FoxO3信号通路,有效改善Aβ病理,展现出对AD潜在疗效。这项研究不仅为活细胞线粒体自噬的精准评估提供了新工具,也为神经退行性疾病的机制研究和药物筛选开辟了新路径。
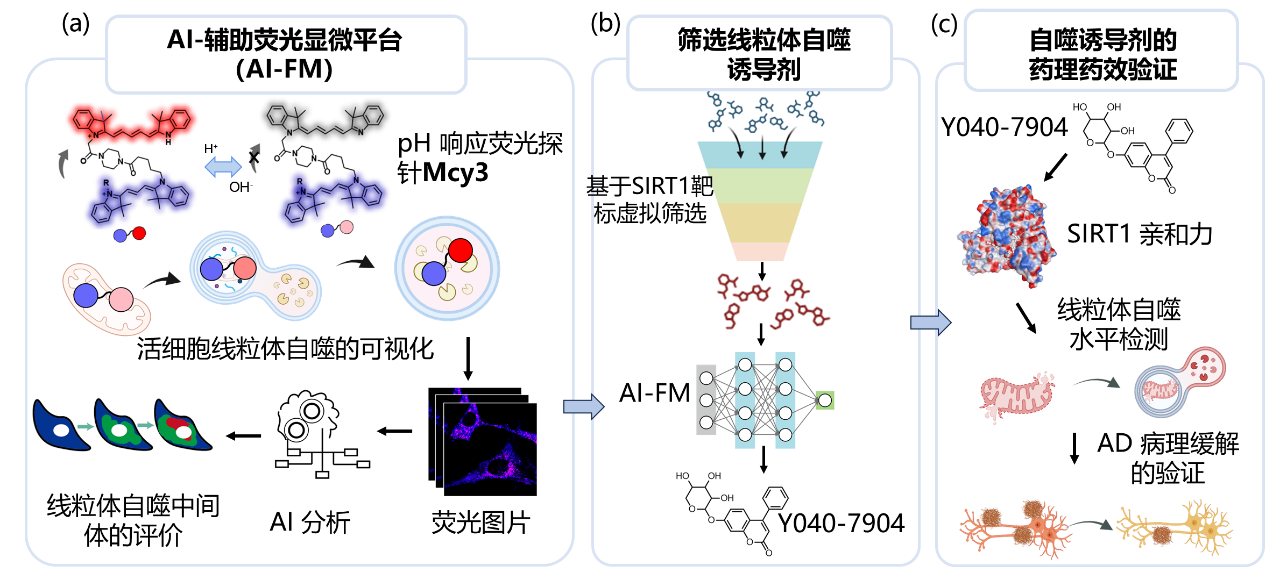
图1. AI辅助荧光显微平台推动线粒体自噬诱导药物的高效筛选
复旦大学药学院博士生王艺澄、信息科学与工程学院博士生宋鹏斐、药学院博士生周荷清为本文共同第一作者。复旦大学药学院李聪教授、游艳青年研究员,复旦大学信息科学与工程学院余锦华教授,以及云南大学药学院雷祖海教授为本文的通讯作者。该工作获得国家重点研发项目,国家自然科学基金项目,上海市“科技创新行动计划”细胞与基因治疗专项项目和复旦大学AI for Science项目支持。
原文链接:https://www.nature.com/articles/s41467-025-60315-1


