癫痫是一种常见的神经功能障碍性疾病,全球人口患病率接近1%,每年新增近500万。虽然目前临床批准20多种抗癫痫药,但仍有约30%癫痫患者无法通过药物有效控制,被称为难治性癫痫。相比普通癫痫患者,难治性癫痫患者伴有认知发育障碍,严重的社会歧视,死亡率和经济负担也显著增加。手术切除致痫灶是治疗难治性癫痫最有效的方法,相比于药物治疗,可使患者死亡率下降约3倍,无发作可能性提高25倍。准确定位致痫灶是实施手术干预的前提。临床常用脑电图、磁共振成像、正电子发射断层扫描、单光子发射计算机断层扫描等技术定位致痫灶,但由于癫痫的异质性和致痫灶隐匿性,临床仅有不到1%的癫痫患者最终接受了手术治疗。因此,开发可反映致痫灶演进的生物标志物并构建特异性良好的分子探针是致痫灶可视化的关键。
复旦大学药学院李聪教授团队对近年报道的致痫灶生物靶标和分子探针进行了系统介绍,该工作以题为《定制材料实现癫痫可视化:从生物标志物到影像探针》(Tailoring Materials for Epilepsy Imaging: From Biomarkers to Imaging Probes)综述文章发表在《先进材料Advanced Materials》杂志。该工作首先总结了癫痫演进过程中潜在生物标志物并将其分为功能异常、分子异常和结构异常三类,继而介绍了用于构建分子探针的材料及其病灶定位性能和优势,最后讨论了下一代癫痫探针发展前景及其在临床转化中的挑战。
致痫灶生物标志物的确定是探针设计的前提。癫痫发生(epileptogenesis)是大脑从非癫痫状态逐渐发展为产生自发癫痫放电的动态过程,在时间上可以分为初始阶段(致癫痫变化开始发生)、潜伏阶段(无癫痫发作活动的静默期)和慢性阶段(自发性癫痫反复发作)(图1)。这一过程伴随着细胞功能、代谢分子和组织结构的异常,上述异常有望作为生物标志物定位致痫灶。
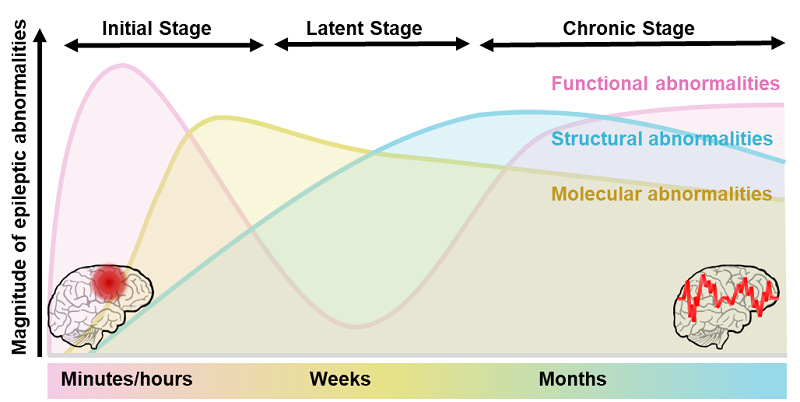
图1. 癫痫发生、发展的病理学发展过程
神经血管单元(neurovascular unit, NVU)由神经元-胶质细胞-血管构成,三者在空间上相互依存,生理上相互影响,是维持神经功能的基本单元。NVU中任何一种细胞功能或分子异常均会产生级联反应,诱发癫痫产生。如图2所示,外部刺激和遗传缺陷累积等风险因素通过破坏NVU稳态触发异常神经元放电,神经元兴奋性活动激活小胶质细胞并释放多种促炎细胞因子,进一步破坏血脑屏障完整性,诱导胶质细胞增生并加深神经元兴奋性,由此形成一个正向反馈回路,促进神经炎症播散,降低神经元放电阙值。
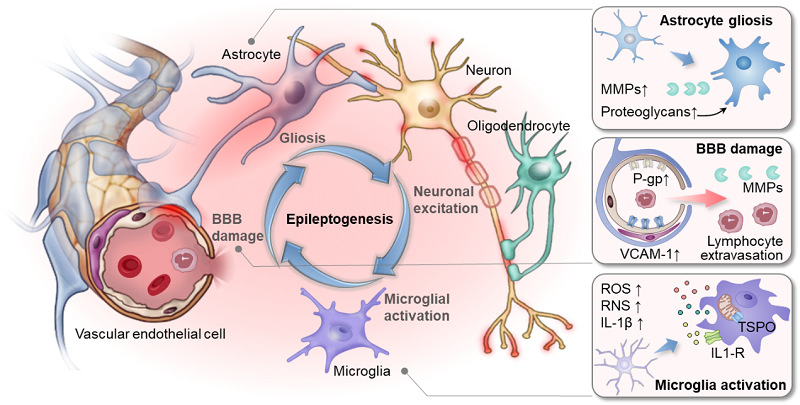
图2.神经血管单元稳态失衡导致神经炎症及癫痫发生的关键事件
分子探针能显著提高致痫灶定位的灵敏度和空间分辨率,生物材料发展从多个方面提升探针性能:(1)优化探针的生物利用度和药物动力学,提高致痫灶成像的特异性和灵敏度;(2)帮助探针克服多重生物学屏障,提高其组织穿透性;(3)赋予探针响应性,实现病灶内信号的开启或放大,提高成像信噪比。该工作将癫痫进展过程中的生物标志物归纳为三类:功能异常、分子异常和结构异常,并介绍了详细介绍了针对上述标志物探针的成像机制,设计方案,及其具体应用(图3)。
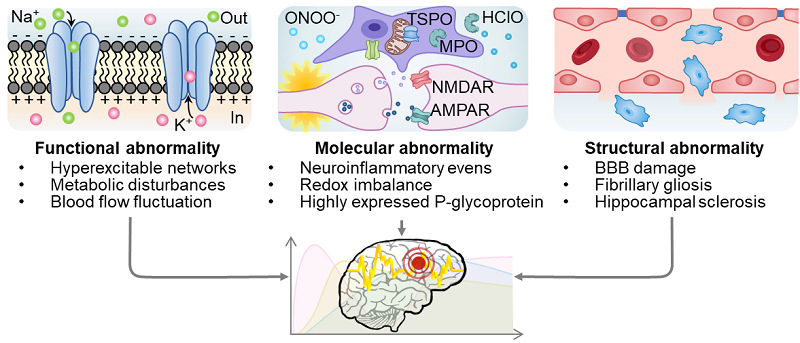
图3. 癫痫病灶部位功能、分子和结构异常为致痫灶定位提供潜在靶标
准确定位致痫灶是难治性癫痫患者实施手术的先决条件,然而目前临床成像技术并不能准确、及时定位致痫灶,导致大多数患者与手术治疗失之交臂。开发新型分子探针是准确定位隐匿型致痫灶的关键,而生物材料的快速发展为构建高灵敏度、高信噪比、生物兼容性好的分子探针提供了新机遇(图4)。展望未来,致痫灶探针的发展主要包括三方面:(1)探索新型致痫灶生物标志物。癫痫病灶异质性及其所处的发展阶段为单一标志物描绘致痫灶带来巨大挑战,探索新的癫痫生物标志物以及多种生物标志物组合有望提高癫痫成像准确性及特异性。(2)构建创新分子探针。合成可响应外源/内源性病理微环境特征的探针有助于提高探针灵敏度及特异性。借助仿生系统、纳米载体等先进材料有助于探针的组织穿透性及其在靶部位的富集。同时,设计比率响应型探针能进一步实现对目标生物标志物的定量测量。(3)开发术中导航分子探针。目前多数报道的癫痫成像探针集中于术前致痫灶定位,可用于术中导航的探针严重匮乏。构建基于近红外荧光、拉曼散射的光学探针有助于实现术中致痫灶准确定位,为降低麻醉对术中脑电准确性影响、提高外科医生手术便利性提供新工具。

图4. 癫痫演进过程中的生物标志物及相关分子探针
复旦大学药学院博士生赵静、王聪博士为该论文的共同第一作者。复旦大学药学院李聪教授为论文的通讯作者。浙江大学医学院博士生孙琬冰参与论文撰写。该工作获得国家重点研发计划,国家杰出青年基金,上海市脑与类脑智能基础转化应用研究市级科技重大专项,上海市科学技术委员会、复旦大学双一流项目,博新计划以及博士后面上等项目的支持。
Abstract: Excising epileptic foci (EF) is the most efficient approach for treating drug-resistant epilepsy (DRE). However, owing to the vast heterogeneity of epilepsies, EF in one-third of patients cannot be accurately located, even after exhausting all current diagnostic strategies. Therefore, identifying biomarkers that truly represent the status of epilepsy and fabricating probes with high targeting specificity are prerequisites for identifying the “concealed” EF. However, no systematic summary of this topic has been published. In this paper, we first summarize the potential biomarkers of EF and classify them into three categories: functional, molecular, and structural aberrances during epileptogenesis, a procedure of non-epileptic brain biasing toward epileptic tissue. The materials used to fabricate these imaging probes and their performance in defining the EF in preclinical and clinical studies are highlighted. Finally, the perspectives for developing the next generation of probes and their challenges in clinical translation are discussed. In general, this review will be helpful in guiding the development of imaging probes defining EF with improved accuracy and holds promise for increasing the number of DRE patients who are eligible for surgical intervention.
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202203667