小胶质细胞作为大脑驻留免疫细胞,构成了大脑的主要防御系统,它们在多种生理与病理过程中发挥着关键作用,如突触修剪、病原体吞噬、神经元兴奋性调节、凋亡细胞清除和免疫微环境形成等。为了实现其功能多样性,小胶质细胞展现出多种极化状态,包括抵抗病原体的促炎表型和促进组织修复的抑炎表型。小胶质细胞表型的多样性与脑部疾病的发病机制、免疫微环境调节和神经炎症水平的波动均密切相关。因此,实现小胶质细胞表型可视化对于了解脑部疾病进展、实时监测神经免疫微环境,以及动态评估候选药物预后至关重要。尽管已有多种针对神经炎症相关受体被报道,包括转运蛋白18kDa(TSPO)、环氧化酶(COX1/2)、集落刺激因子1受体(CSF1R)和嘌呤能受体P2X7,但上述靶点及其探针仍面临局限性:(1)相关受体在多种脑细胞中均有表达,导致探针特异性降低;(2)无法有效区分活化小胶质细胞的不同表型,从而限制了其对免疫炎性微环境评估的准确性;(3)探针难以高效入脑。因此,开发特异表型小胶质细胞靶向PET探针是临床亟待解决问题。P2Y12是仅表达在小胶质细胞膜表面的嘌呤能受体,且其表达水平具有表型依赖性,在抑炎小胶质细胞中表达水平显著高于促炎表型。因此,构建P2Y12受体靶向PET探针对反映脑部疾病相关小胶质细胞表型转化、神经免疫微环境和急性炎症进展均有重要意义。

近日,复旦大学药学院李聪教授、王聪青年研究员和复旦大学附属华山医院神经外科张新主治医师在Acta Pharm Sin B(药学学报B)杂志以封面发表了题为:“Synthesis, Preclinical Evaluation, and Pilot Clinical Study of a P2Y12 Receptor Targeting Radiotracer [18F]QTFT for Imaging Brain Disorders by Visualizing Anti-Inflammatory Microglia”(P2Y12受体靶向放射性探针[18F]QTFT的合成、临床前评价和探索性临床研究-可视化抑炎表型小胶质细胞定位脑部疾病)研究型论文。该工作构建了靶向嘌呤能受体(P2Y12)的小分子PET探针[18F]QTFT,其不但对P2Y12受体具有高亲和力(14.43 nmol/L),而且还表现出较好的血脑屏障通透性,实现了抑炎表型小胶质细胞相关多种脑部疾病可视化。该论文被Acta Pharm Sin B杂志选为当期封面论文,并邀请了海军军医大学盛春泉教授对该工作进行专栏评述。
在这项工作中,研究团队以P2Y12受体抑制剂AZD1283为先导化合物,通过计算机辅助设计和模拟了四种P2Y12配体的结构,并设计了标记前体合成和放射性核素标记路线。由6-氯-5-氰基-2-(三氟甲基)烟酸乙酯或6-氯-5-氰基-2-甲基烟酸乙酯通过五步反应合成四种不同结构的标记前体及其19F标准品。进一步,在18F放射性标记中,由18F负离子对前体化合物的取代基团(-OTs)进行SN2亲核反应得到18F放射性标记的P2Y12探针(图1)。
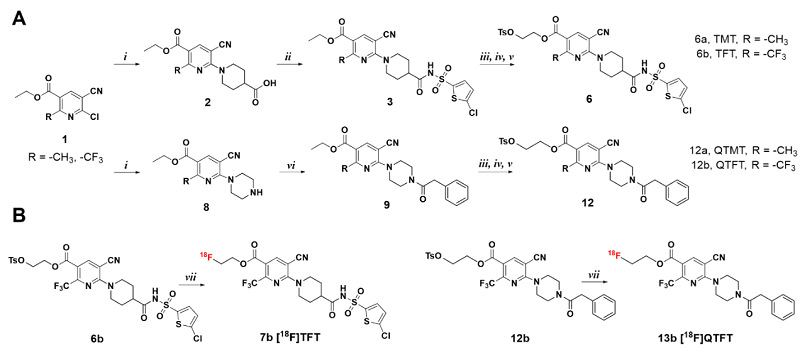
图1. 靶向P2Y12放射性示踪剂的合成。(A)TMT、TFT、QTMT和QTFT前体的合成。(i)3-氮环丁酸,DIPEA,乙醇,60 ℃,1小时;(ii)5-氯噻吩-2-磺酰胺,EDC,HOBT,DIPEA,二氯甲烷,0 ℃至常温,24小时;(iii)氢氧化锂(1.0 M),四氢呋喃,水,常温,3 小时; 乙醇,50 ℃,12 h;(iv)乙二醇,EDC,DMAP,二氯甲烷,0 ℃至常温,5小时;(v)对甲苯磺酰氯,DMAP,吡啶,0 ℃至常温,3小时;(vi)哌嗪,DIPEA,乙醇,60 ℃,1小时。(B)[18F]TFT和[18F]QTFT的放射合成。(vii)18F-,K2.2.2,碳酸钾,乙腈,10分钟。
中枢神经系统PET放射性示踪剂的血脑屏障通透性通常受分子理化特性的影响,例如拓扑极性表面积(TPSA)、分子量、亲脂性、pKa、游离氢键、血浆蛋白结合和外排转运蛋白。四种配体的理化参数如表1所示,低TPSA和较高的亲脂性值表明QTFT和TFT的结构具有理想的血脑屏障通透性和受体亲和力。
表1 P2Y12配体理化参数
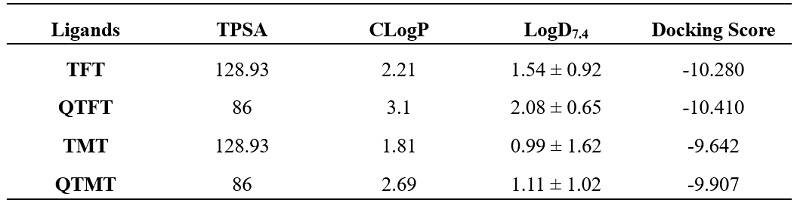
为了解结构-功能关系,研究团队利用计算机辅助设计分析配体与受体蛋白的结合模式。对接结果输出配体-受体蛋白的结合能为相应的对接分数,较低的结合能预示配体结构与受体蛋白具有较高的结合亲和力。计算得到QTFT和TFT的对接分数较低,具有较好的亲和力。通过18F放射性标记得到[18F]TFT和[18F]QTFT,放射化学纯度(RCP)大于95%。衰变校正后计算得到[18F]TFT和[18F]QTFT的放射化学产率(RCY)分别为9.9±1.5%和10.3%±1.1%,比活度为80‒120 GBq/μmol。通过放射性HPLC测定两种探针在生理盐水和小鼠血清中的体外稳定性,结果显示共孵育4小时后没有明显放射性分解。此外,[18F]QTFT的小鼠体内稳定性结果表明,给药后2小时依旧未检测到明显的游离18F或代谢分解物(图2)。
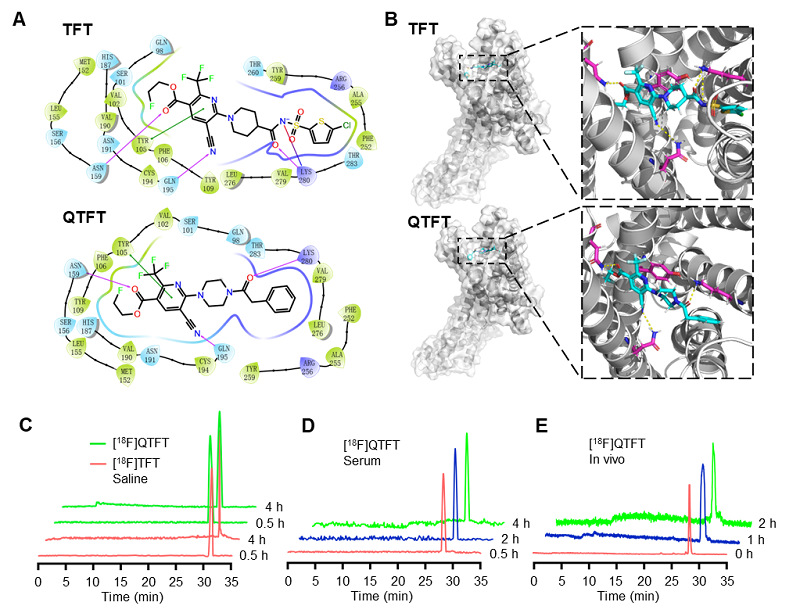
图2. [18F]TFT和[18F]QTFT 表现出较高的代谢稳定性。(A)TFT和QTFT的2D结合模式。(B)TFT和QTFT与P2Y12受体结合的共晶结构(PDB ID:4PXZ)。(C)[18F]QTFT和[18F]TFT在盐水中的体外稳定性。(D)[18F]QTFT在小鼠血清中的体外稳定性。(E)[18F]QTFT在体内稳定性。
研究团队使用膜结合试验评估了[18F]TFT和[18F]QTFT与P2Y12受体的结合亲和力,[18F]TFT的解离常数(Kd)为6.55 nmol/L,而[18F]QTFT的解离常数(Kd)为14.43 nmol/L。在高表达P2Y12受体的C6胶质母细胞瘤细胞系中,研究[18F]TFT和[18F]QTFT的时间依赖性细胞摄取,结果表明探针随孵育时间的延长而增加。此外,加入过量的P2Y12受体抑制剂氯吡格雷后,细胞摄取量显着降低。为了有效地进行脑部疾病成像,放射性示踪剂必须有效穿过血脑屏障,并且不会被P-糖蛋白(P-gp)泵出。Transwell试验结果显示[18F]QTFT的透过率达到19.6%,而[18F]TFT的透过率仅为7.5%,表明[18F]QTFT具有较好的血脑屏障穿透性。在使用P-gp抑制剂维拉帕米后,[18F]TFT渗透效率显着提高至17.2%,而[18F]QTFT仅略微提高至21.5%。这些结果表明,P-gp阻断显着增加了[18F]TFT的跨膜量,而对[18F]QTFT的影响却很小,说明[18F]QTFT不是P-gp的强结合底物,有利于脑部PET成像研究(图3)。
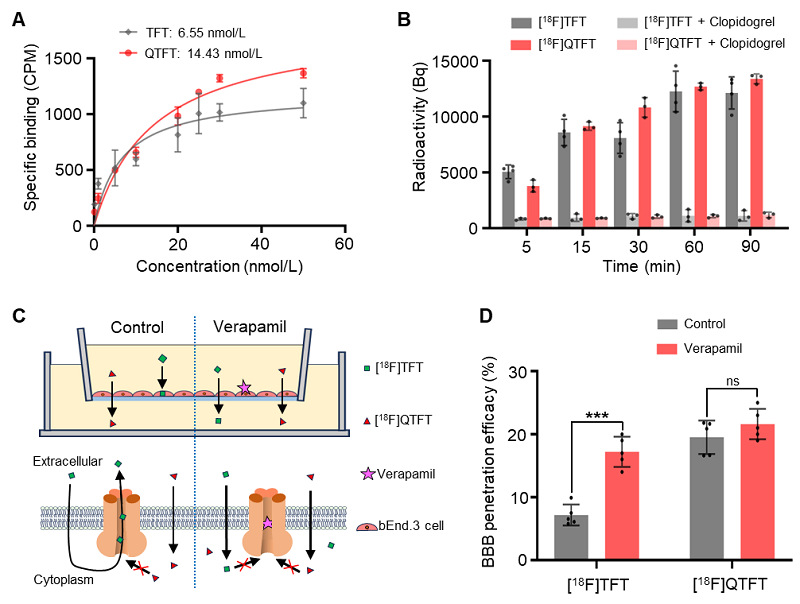
图3. [18F]QTFT显示高血脑屏障通透性和对P2Y12受体的结合亲和力。(A)使用高表达P2Y12受体的C6细胞测定[18F]TFT和[18F]QTFT的结合亲和力。(B)[18F]TFT和[18F]QTFT的时间依赖性C6细胞摄取及抑制。(C)体外Transwell评估[18F]TFT和[18F]QTFT的血脑屏障通透性示意图。(D)体外Transwell评估[18F]TFT和[18F]QTFT的血脑屏障通透性。
随后,研究团队在正常小鼠上进行体内动态PET/CT成像研究,结果表明[18F]TFT和[18F]QTFT在脑摄取方面存在差异,[18F]QTFT表现出更高的脑部摄取。[18F]QTFT的SUV峰值达到1.77±0.27,而[18F]TFT仅为0.44±0.34。另外,[18F]QTFT的平均保留水平为SUVmean = 0.69±0.11,而[18F]TFT仅达到0.12±0.08。这些结果表明,[18F]QTFT在血脑屏障穿透性和脑摄取方面优于[18F]TFT。此外,为了在体内验证[18F]QTFT对P2Y12受体的体内特异性。通过使用阻断剂QTFT,脑部[18F]QTFT的SUV降低了72.3%。因此,[18F]QTFT是兼具血脑屏障穿透性和高P2Y12受体结合亲和力的放射性示踪剂(图4)。
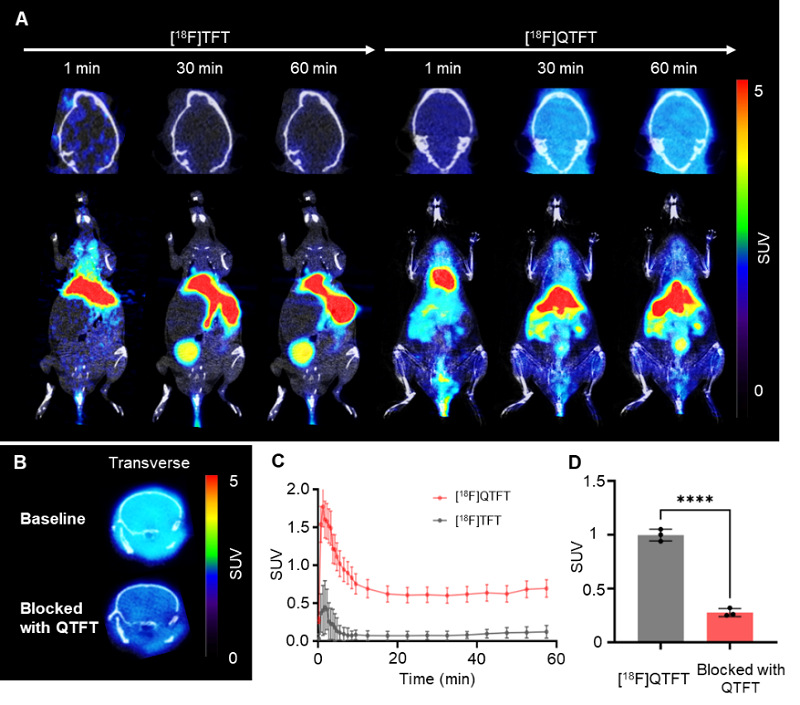
图4. [18F]QTFT显示脑部摄取水平高于[18F]TFT。(A)[18F]QTFT和[18F]TFT的动态PET/CT成像正常C57BL/6小鼠。(B)[18F]QTFT的静态PET/CT成像正常C57BL/6小鼠和QTFT阻断后成像。(C)[18F]QTFT和[18F]TFT的动态PET/CT成像的时间-活度曲线(TAC)。(D)[18F]QTFT的静态PET/CT成像和QTFT阻断后成像脑部标准化摄取值(SUV)。
为了验证[18F]QTFT的P2Y12受体靶向特异性,研究团队分别构建了脑部原位LPS诱导的促炎和IL-4诱导的抑炎小鼠模型。LPS诱导组在大脑中未表现出任何明显的信号变化,而IL-4诱导组在诱导的病灶内表现出信号升高,但在对侧大脑中升高不明显。在使用P2Y12抑制剂氯吡格雷(1.0 mg/kg)阻断后,观察到PET信号降低约1.45倍,表明[18F]QTFT的高特异性。收集来自LPS诱导和IL-4诱导的脑组织样本进行免疫荧光染色,IL-4诱导区中P2Y12的表达增加,这证实[18F]QTFT可以成像抑炎表型小胶质细胞(图5)。
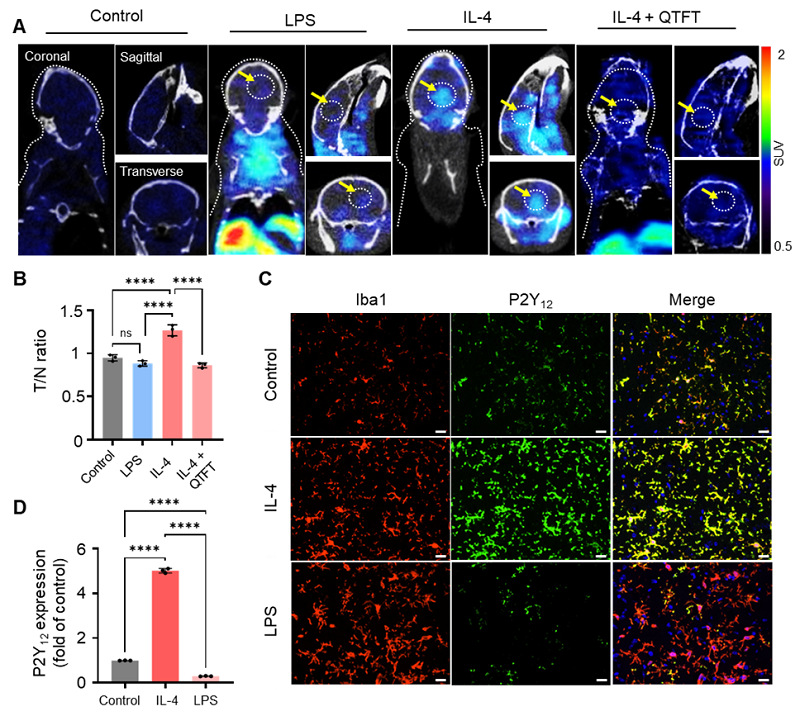
图5. [18F]QTFT可视化小胶质细胞抗炎表型极化。(A)[18F]QTFT PET/CT成像LPS-/IL-4诱导的小鼠模型。(B)对照组、LPS诱导组、IL-4诱导组和QTFT阻断IL-4诱导组的脑组织中[18F] QTFT的T/N比值。(C)对照组、LPS诱导组、IL-4诱导组和QTFT阻断IL-4诱导组的脑组织的免疫荧光染色。(D)对照组、LPS诱导组、IL-4诱导组和QTFT阻断IL-4诱导组的脑组织中P2Y12表达水平的定量。
反应性小胶质细胞在癫痫发生过程中会表现出多种功能表型,因此研究团队首先在小鼠海马区域注射红藻氨酸构建癫痫小鼠模型。同时,在相应的癫痫分期记录脑电图(EEG)(急性:癫痫持续状态(SE)后1-3天;潜伏期:SE后8-20天;慢性:SE后20-180天)。并随后进行[18F]QTFT PET研究,结果表明[18F]QTFT PET在急性期癫痫小鼠模型的同侧海马体中显示出高信号(注射后60分钟T/N值=1.81±0.22)。相反,潜伏期和慢性期癫痫小鼠模型中的摄取相对较低(T/N值=1.14±0.05 和1.12±0.03)。癫痫小鼠脑组织的尼氏染色显示,在癫痫的急性期,神经元显著丢失,而在慢性期略有增加。癫痫脑组织的免疫荧光染色显示P2Y12受体在急性期上调(图6)。
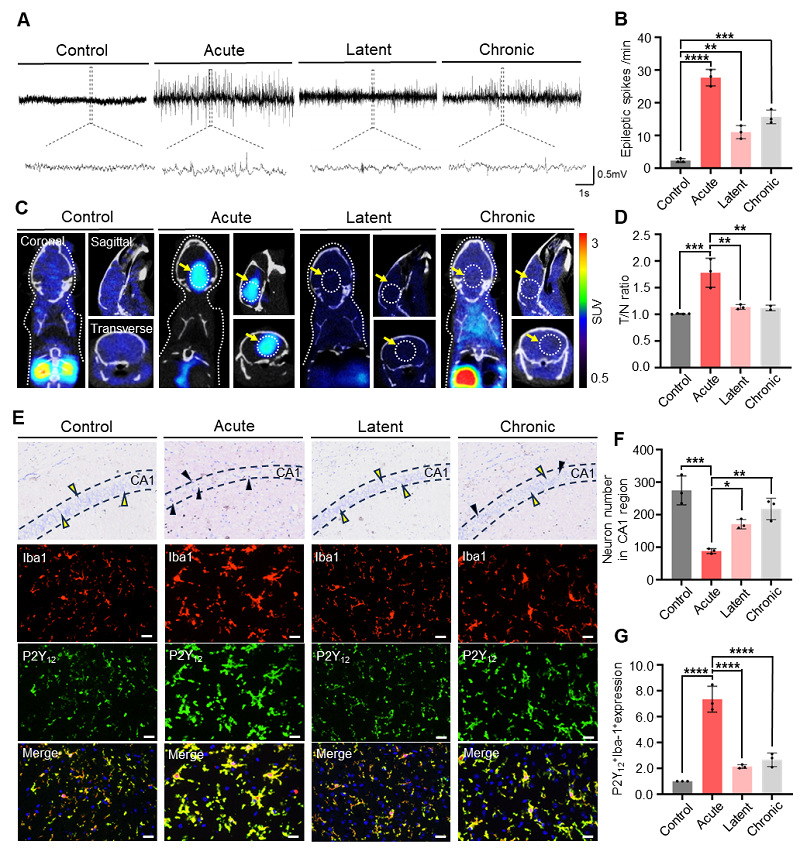
图6. [18F]QTFT通过定位抗炎小胶质细胞可视化癫痫病灶。(A)对照组、急性期组、潜伏期组和慢性期组癫痫小鼠模型的脑电图。(B)急性期、潜伏期和慢性期癫痫模型中的癫痫波峰数。(C)对照组、急性期组、潜伏期组和慢性期组癫痫小鼠模型[18F]QTFT PET/CT图像。(D)对照组、急性期组、潜伏期组和慢性期组的T/N比值。(E)对照组、急性期组、潜伏期组和慢性期组脑组织的尼氏染色和免疫荧光染色。(F)CA1区域中神经元数量。(G)P2Y12和Iba1均阳性表达的细胞统计。
衰老是导致神经退行性疾病的最大的风险因素之一,因此,了解小胶质细胞随衰老而转化的时空动态对于预防或治疗与年龄相关的疾病至关重要。研究团队为了可视化衰老小鼠中小胶质细胞P2Y12表达的差异,利用[18F]QTFT对6、40和60周小鼠的小鼠模型进行了动态PET/CT成像分析,结果显示[18F]QTFT 6周年轻小鼠的大脑中表现出更高的摄取率(SUV=0.61±0.06),而在40周和60周龄中,SUV分别为0.52±0.04和0.45±0.06。这些结果表明,[18F]QTFT定量衰老过程中P2Y12受体表达的降低。(图7)。
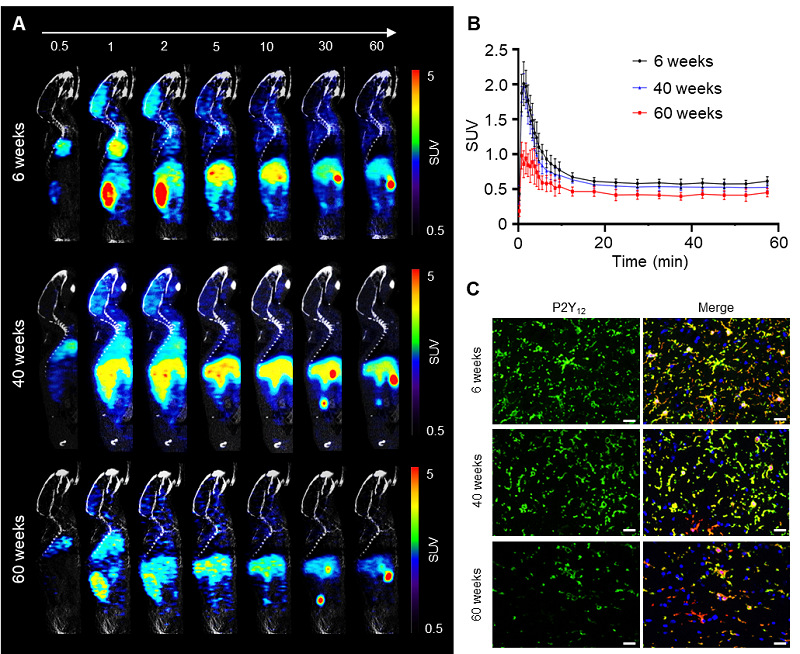
图7. [18F]QTFT定量老年小鼠大脑中抗炎小胶质细胞的减少。(A)6、40和60周小鼠的[18F]QTFT动态PET/CT图像。(B)6、40和60周小鼠的脑部摄取的时间-活度曲线(TAC)。(C)6、40和60周小鼠的脑组织样本中小胶质细胞免疫荧光染色。
神经胶质瘤是成人中最常见的恶性脑肿瘤,其免疫抑制微环境与小胶质细胞的抗炎转化密切相关。抗炎小胶质细胞可产生生长因子,增强神经胶质瘤细胞增殖,减少神经胶质瘤细胞凋亡,促进肿瘤细胞迁移。因此,抗炎小胶质细胞的PET成像将有助于脑神经胶质瘤的定位和免疫治疗的评估。研究团队首先通过颅内注射GL261细胞构建神经胶质瘤小鼠模型,并使用T2加权MRI确认肿瘤形成。随后,利用[18F]QTFT对神经胶质瘤进行成像,并将其与临床应用的肿瘤氨基酸代谢示踪剂[18F]FET进行比较。结果显示,与[18F]FET相比,[18F]QTFT在肿瘤检测中表现出更高的靶本比。[18F]QTFT的T/N值为1.47±0.01,高于[18F]FET(1.17±0.02)。免疫荧光染色进一步证实[18F]QTFT特异性地对表达P2Y12受体的小胶质细胞进行成像(图8)。
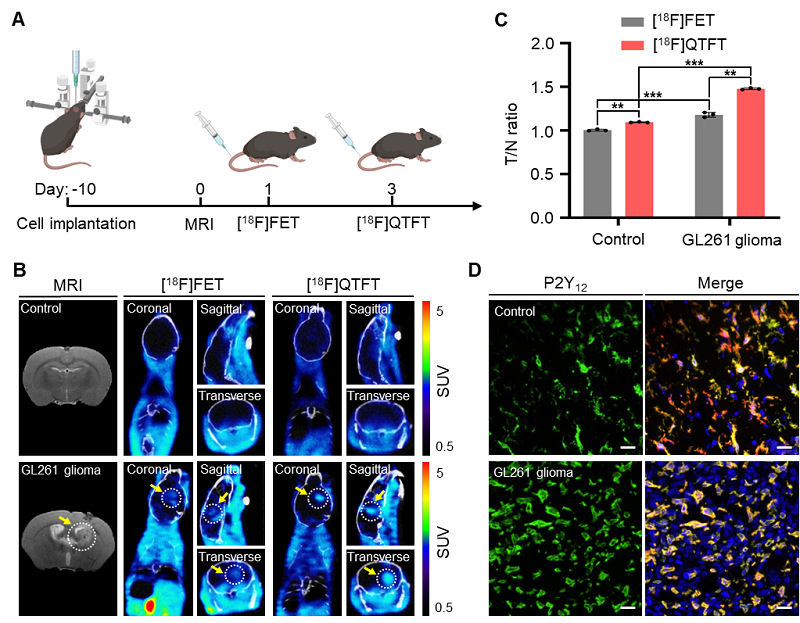
图8. [18F]QTFT可视化原位神经胶质瘤。(A)GL261神经胶质瘤小鼠模型构建和PET成像示意图。(B)对照组和胶质瘤模型组的MRI成像、[18F]FET和[18F] QTFT PET/CT成像。(C)[18F]FET和[18F]QTFT PET成像胶质瘤的T/N值。(D)对照组和胶质瘤模型组的正常脑和肿瘤组织的免疫荧光染色。
为了进一步评估探针临床转化潜力,研究团队对颞叶癫痫患者进行了[18F]QTFT PET成像。首先在T2加权MR图像上观察到右颞叶病变。其次,应用临床癫痫诊断的γ-氨基丁酸受体(GABAA)靶向的18F-氟马西尼([18F]FMZ),PET成像显示病变区域为低摄取信号(癫痫灶SUVmean=0.54±0.28),对侧正常大脑(SUVmean=5.45±0.35)。随后,[18F]QTFT动态PET成像显示癫痫灶中的信号强度较高(SUVmean=1.29±0.28),而对侧正常大脑区域的SUVmean为0.90±0.16。这些结果表明[18F]QTFT用于定位癫痫患者的癫痫病灶的临床潜力(图9)。
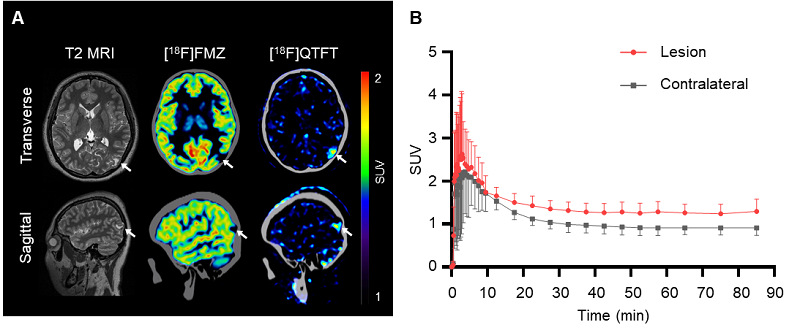
图9. [18F]QTFT对癫痫患者癫痫灶的PET成像。(A)T2 MR成像、[18F]FMZ和[18F]QTFT成像颞叶癫痫患者。(B)颞叶癫痫患者的病灶和对侧正常大脑摄取的时间-活度曲线(TAC)。
综上,本工作构建了一种小分子PET探针[18F]QTFT,该探针具有对P2Y12受体的高亲和力和血脑屏障高通透性,实现了对抑炎表型小胶质细胞相关多种脑部疾病的可视化和临床应用。主要创新点在于:(1)构建了靶向P2Y12受体的分子探针,为抑炎表型小胶质细胞在体定量提供了影像工具;(2)实现了癫痫致痫灶定位和衰老动物模型的病理分期,为脑部疾病神经炎症的表型划分提供了新策略;(3)初步评估该探针在临床患者癫痫病灶的定位潜力,为小胶质细胞表型靶向探针在临床的脑部病灶诊断和神经免疫微环境评价提供了新角度。
复旦大学药学院博士生姚博霖、复旦大学附属华山医院副主任医师孔艳艳、复旦大学药学院博士生李嘉宁、复旦大学附属闵行医院主任医师徐福林为本文共同第一作者。复旦大学药学院李聪教授、复旦大学药学院王聪研究员和复旦大学附属华山医院神经外科张新主治医师为本文共同通讯作者。该工作获得国家科技部重点研发项目,上海市科委计划项目,国家杰出青年科学基金,国家自然科学基金项目和上海市科技项目的支持。
原文链接:https://www.sciencedirect.com/science/article/pii/S2211383525000140